2020年5月,医疗器械CE认证法规将开始在欧盟申请(法规(EU)2017/745),该法规于2017年生效,并废除了之前的现行指令。它意味着对公司的新要求并涵盖更多产品,因此,在这个新的截止日期临近时,谨慎是至关重要的。
新的医疗器械法规?
1、范围更广
随着新的医疗器械法规在欧盟生效,现在涵盖了更多的产品。具有非医疗目的的医疗器械现在属于法规范围。
具有美学目的的这些装置列于该法规的附件XVI中,并且可能在临界产品方面存在问题(在两个法规之间)。这些附件XVI产品可以是例如强脉冲光设备,乳房假体,或甚至具有美学目的的隐形眼镜。
其他法规之间也存在边界产品。例如,可以考虑口腔护理产品,这取决于产品,医疗装置或化妆品。我们即将发布一篇关于医疗器械临界产品的文章,以便更容易识别。
2、新的分类规则
分类修改很重要,该规定将分类规则的数量从18个增加到22个,旧的指令I类设备现在可能被视为IIa类,具有这一新规定。预计截止日期和谨慎是必不可少的。
3、加强监督
欧洲法规的主要目标仍然是保护消费者。在这里,它更具体地协调了设备安全方面的要求。
一个更好的市场预评估现在需要。为此,必须提供更多信息和数据。每个州的通知机构现在都处于欧洲控制之下,保证每个州都有相同的要求标准。
上市后安全监测也得到了改善。公司不仅需要定期报告设备安全性,而且还将在欧洲范围内实施新的监控工具。
实际上,欧洲联盟目前正在开发一个欧洲医疗设备数据库--EUDAMED,它应该在2020年3月25日之前投入使用。后者将允许经营者来注册自己和医疗设备,同时也集中临床研究,警惕,市场监管等。当然,所有的数据将不会被公开。此数据库将与唯一设备标识符(或UDI)系统一起使用。UDI将由设备标识符和生产单元标识符组成。
截止日期和关键日期
该规定将于2020年5月26日起实施,其中准指令以完整的形式废除,但还有其他日期需要记住。这是一个快速摘要:
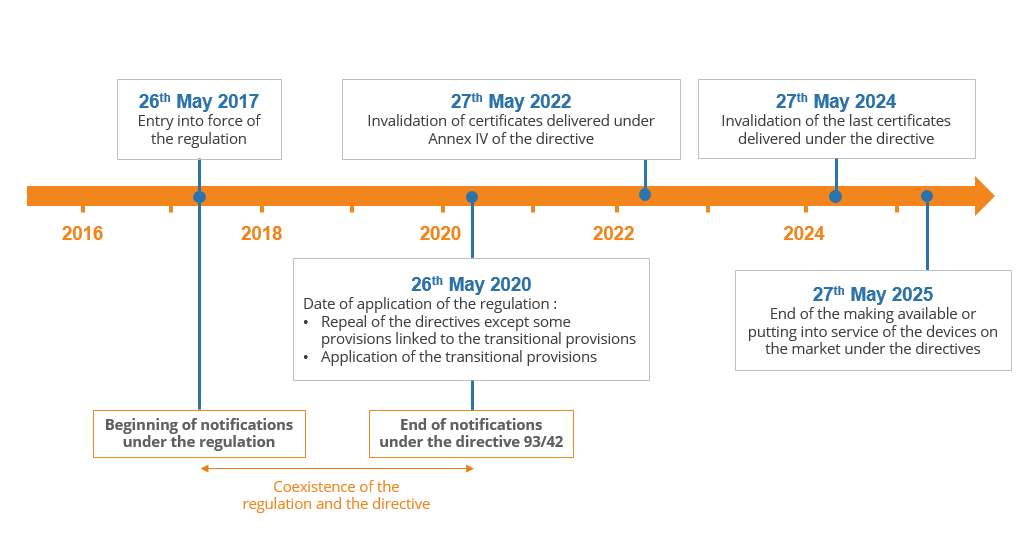
该法规的实施将持续数年:
1.在申请之日,即2020年5月,所有类别的设备都需要遵守该规定,
2.在2022年至2024年之间,根据指令交付的证书将失效,
3.2024年5月27日,由于最后证书无效,所有IIa至III类医疗器械必须遵守该规定,
4.根据该指令合法商业化的设备仍可在市场上销售或投入使用,直至2025年5月27日。
我们的专家将负责处理从I级到IIa级的医疗设备的注册。由于他们对这项新法规的深入了解,我们的专家会为您提供最佳预测未来期限的策略建议。
背景:为什么这个规定?
迄今为止,欧洲指令规定医疗器械的营销可追溯到1990年,对于最老的医疗器械。作为指令,它们没有直接适用性,因此必须转换为每个州的国家立法。
因此,每个成员国都可以自由地解释文本,从而在其应用中产生差异。
一个监管然而,有直接适用于所有成员国,并允许这个原因,统一的要求,关于医疗器械的销售。
